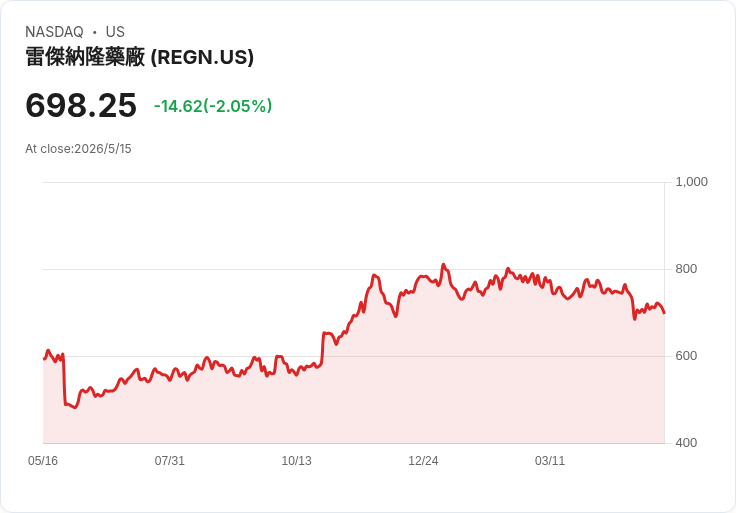
Regeneron 的 fianlimab+cemiplimab 對比 pembrolizumab 第三期試驗未達統計顯著之無進展生存期(PFS)。
Regeneron 今(週五)宣佈,其評估 fianlimab 與 cemiplimab(Libtayo)聯合療法對比 pembrolizumab(Keytruda)作為第一線治療的第三期臨床試驗,未能以統計顯著性達成主要療效終點——無進展生存期(PFS)。該試驗共納入超過 1,500 名年齡 12 歲以上、無法手術切除之區域性晚期或轉移性黑色素瘤患者,且測試了兩個劑量水準的聯合療法。公司同時指出,該組合未顯示新的安全性警訊。
背景與脈絡: 近年來抗 PD‑1 類藥物(如 Merck 的 pembrolizumab/Keytruda、Regeneron 的 cemiplimab/Libtayo)已成為多類腫瘤的一線治療基礎;業界也積極探索與其他免疫檢查點抑制劑(如 LAG‑3 抑制劑)之聯合,以期提高反應率與延長病人存活。此次試驗評估的正是以不同檢查點聯手的策略,試圖在首線治療中對抗 Keytruda 的市場與療效領先地位。
事實與細節: - 試驗規模:超過 1,500 名受試者,年齡 ≥12 歲,病況為不可切除之區域性晚期或轉移性黑色素瘤。 - 比較物件:fianlimab + cemiplimab(兩個劑量層級)與 pembrolizumab 單藥治療。 - 主要結果:未以統計學上顯著差異達成 PFS 主要終點。 - 安全性:公司未觀察到新的安全性訊號。 - 進行中研究:另一項第三期試驗正比較 fianlimab + cemiplimab 與 Bristol Myers 的 Opdualag(另一款組合療法)。
深入分析與意義: 這項結果對 Regeneron 的黑色素瘤開發計畫構成重大挫折。主要原因在於,首次一線治療要取代或優於現行標準(如 pembrolizumab)門檻高,必須在整體族群中展現清晰且穩定的 PFS 或整體存活(OS)利得。雖然安全性報告為正面,但療效端未達標意味著短期內難以改變治療指引或取得市場優勢。此外,超過千人的大型試驗失利,可能迫使公司重新檢視劑量、病人分層、或生物標記導向的治療策略。
替代觀點與駁斥: 支持者可能指出:初步失敗不代表完全無效,仍需等待次要終點、OS 資料或亞群分析,或許在特定病人群(例如帶有特定生物標記者)有顯著效益。這一點成立,但必須強調:若主要終點在整體族群未達標,短期內該療法要取得廣泛適應症或改變臨床常規的可能性仍受限;子群益處需被嚴格驗證且往往需額外試驗支援。
後續展望與行動呼籲: 投資者與醫療界應關注公司將釋出的完整資料與亞群分析,這些結果將決定是否有可行的救濟路徑(如針對特定患者群的適應症申請或改良方案)。同時,Regeneron 與合作夥伴需評估正在進行中對 Opdualag 的試驗是否需調整設計或策略。對於臨床醫師與病人,應持續關注多中心資料與後續研究結果,避免過早改變治療選擇。最後,該結果亦提醒業界:免疫療法組合雖具吸引力,但臨床證據仍是關鍵,需以嚴謹試驗設計與病人分層來提高成功率。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37

 發表
發表


 我的網誌
我的網誌